医药网4月16日讯 日前,四川汇宇制药以仿制4类申报的注射用硼替佐米、盐酸帕洛诺司琼注射液上市申请获得CDE承办受理,至今公司已有11个注射剂以新注册分类报产,其中6个在欧盟获批上市,转报国内并纳入/拟纳入优先审评,此外还有3个欧盟上市注射剂待转报国内。11个注射剂中有3个获批生产并视同过评,培美曲塞为首批4+7品种,借助独家中标优势,汇宇制药市场份额激增;在审的8大注射剂中,汇宇制药的普乐沙福注射液有望以首仿+过评获批上市。
比肩恒瑞、中生,3大品种领跑注射剂过评榜
图:过评注射剂品种数达2个及以上的企业(以集团计)
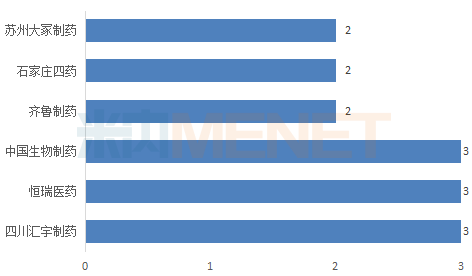
米内网数据显示,目前有企业通过或视同通过一致性评价的注射剂有46个受理号(以
名称计,共30个品种),涉及26家企业(以集团计),其中有6家企业过评注射剂品种数达2个及以上,汇宇制药、恒瑞
、中国生物制药以3个过评品种并列榜首,涉及的受理号分别为7个、3个、3个。
表1:汇宇制药已过评品种
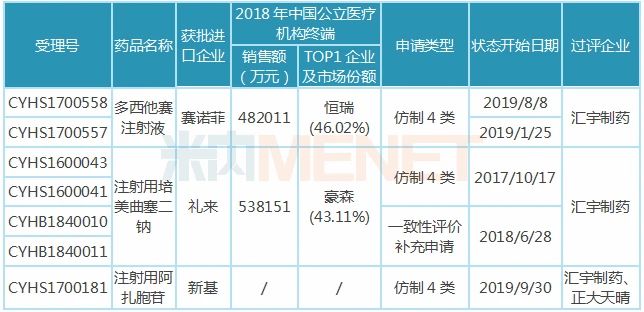
汇宇制药已过评的3款注射剂均为抗肿瘤药,米内网数据显示,2018年中国城市公立医院、县级公立医院、城市社区中心以及乡镇卫生院(简称中国公立医疗机构)终端抗肿瘤化药产品竞争格局中,注射用培美曲塞二钠、多西他赛注射液分别以6.77%、6.06%市场份额排位第一、第二。
3款注射剂中,注射用培美曲塞二钠被纳入第一批4+7带量采购,作为该品种唯一过评
,汇宇制药成功中标。在集采之前,培美曲塞市场主要由豪森、齐鲁及礼来占领,带量采购助力“光脚企业”汇宇制药销量迅速上升,抢占市场份额。
米内网数据显示,2019年重点城市公立医院化学药终端(样本覆盖北京、哈尔滨、长春、沈阳、天津、石家庄、太原、广州、深圳、郑州、重庆、武汉、长沙、上海、济南、杭州、南京、福州、成都、西安20个城市,其中9个为4+7试点城市)注射用培美曲塞二钠厂家竞争格局中,汇宇制药排位第三(销售额同比增长32509.46%),仅次于豪森、齐鲁。凭借独家中标的优势,汇宇制药的市场份额由2018年的0.06%上升至2019年的19.87%。2019年9月开展的4+7扩面集采,汇宇制药与礼来中选,销量有望再上新台阶。
注射用阿扎胞苷过评企业包括汇宇制药及正大天晴,大概率入选第三批国家集采,而多西他赛注射液目前虽仅汇宇制药独家过评,但已有4家药企按仿制4类报产,6家药企提交一致性评价补充申请,不日将诞生第二家过评企业。随着国家带量采购的不断推进,“光脚企业”汇宇制药或将持续受益。
8大注射剂在审,与扬子江、齐鲁等交锋
4月8日、4月10日,四川汇宇制药以仿制4类提交的盐酸帕洛诺司琼注射液、注射用硼替佐米上市申请获得CDE承办受理,至今公司已按新注册分类提交11个注射剂上市申请(3个已获批)。这11个注射剂中,有6个扬子江已布局,齐鲁、正大天晴、恒瑞均布局了5个。
表2:四川汇宇制药新注册分类报产且暂未获批的品种
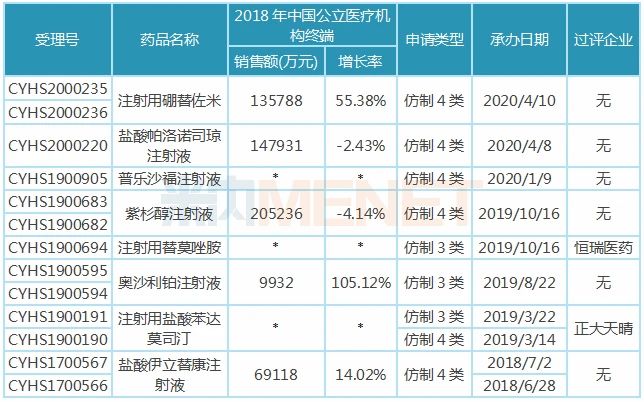
注:销售额低于3000万用符号*代表
在审的8大注射剂中,除了盐酸帕洛诺司琼注射液为止吐止恶心药外,其余7个注射剂均为抗肿瘤药,紫杉醇注射液、注射用硼替佐米年销均超10亿元,在2018年中国公立医疗机构终端抗肿瘤化药产品竞争格局中,分别以2.58%、1.71%排在第16、17位。
注射用替莫唑胺、注射用盐酸苯达莫司汀已有企业过评,恒瑞医药打破了替莫唑胺注射剂型在国内市场的空白局面;正大天晴的注射用盐酸苯达莫司汀以首仿+过评的方式获批上市。
表3:汇宇制药已报产且未有企业过评的品种
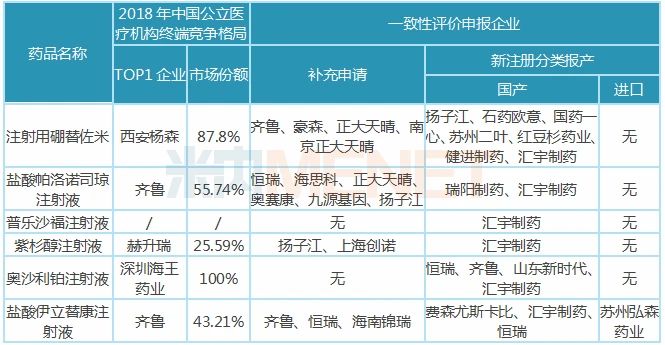
暂无企业过评的6大注射剂中,普乐沙福注射液未有首仿获批,该产品由赛诺菲旗下的健赞制药研发,于2008年12月获得FDA批准上市,2018年12月获批进入国内市场。汇宇制药独家申报,有望以首仿+过评获批上市。
汇宇制药的紫杉醇注射液以新注册分类报产,虽然还有扬子江、上海创诺提交该产品一致性评价补充申请,但汇宇制药的产品由国外转报国内且纳入优先审评,从申报进展看,汇宇制药首家过评的几率还是很大的。
6个注射剂弯道超车,这3个待转报国内
汇宇制药秉承成为国际化制药企业的愿景,历经多年发展,国际化布局卓有成效,2014年成为中国第一家通过英国GMP认证的抗肿瘤注射剂生产企业;2015年成为中国第一家以自主品牌的注射剂在欧美发达国家销售的企业......
目前公司有9个注射剂在欧盟国家获批上市,分别为注射用盐酸苯达莫司汀、多西他赛注射液、盐酸多柔比星注射液、盐酸伊立替康注射液、奥沙利铂注射液、紫杉醇注射液、注射用培美曲塞二钠、唑来膦酸注射液及盐酸表柔比星注射液。
表4:汇宇制药纳入/拟纳入优先审评品种
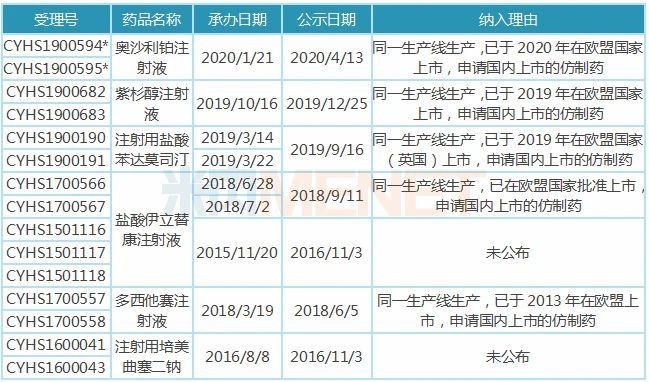
注:带*为拟优先审评
9个注射剂有6个已在国内申报上市,其中5个品种(13个受理号)纳入优先审评,1个品种(2个受理号)拟纳入优先审评,纳入理由为同一生产线生产,已在欧盟国家上市,申请国内上市的仿制药,多西他赛、培美曲塞已顺利获批并视同过评。
表5:汇宇制药已在欧盟上市但未在国内报产的品种

盐酸多柔比星注射液、盐酸表柔比星注射液、唑来膦酸注射液3个品种已在欧盟获批,汇宇制药一旦在国内提交上市申请,将大概率纳入优先审评,实现弯道超车。米内网数据显示,2018年中国公立医疗机构终端多柔比星、表柔比星、唑来膦酸销售额分别为26.85亿元、10.37亿元、20.02亿元。
来源:米内网数据库、公司官网
注:数据统计截至4月15日,如有疏漏,欢迎指正!

 琼公网安备 46010602000893号
琼公网安备 46010602000893号
