恩华儿童新品拟优先审评 独家申报冲击国内首仿
时间:2020-07-16
医药网7月15日讯 7月13日,CDE官网公布最新拟优先审评品种,恩华药业的盐酸咪达唑仑糖浆(受理号CYHS2000375)拟优先审评的理由为“符合儿童生理特征的儿童用药品新品质、剂型、规格”,目前国内市场尚无该产品获批上市,也无其他药企申报上市。
图1:恩华药业的盐酸咪达唑仑糖浆具体情况

来源:CDE官网
米内网数据显示,2019年在中国城市公立医院、县级公立医院、城市社区中心及乡镇卫生院(简称中国公立医疗机构)终端咪达唑仑的销售额为6.3亿元,目前市场上获批的产品包括了马来酸咪达唑仑片、咪达唑仑注射液、咪达唑仑口颊粘膜溶液,注射剂市场份额占比最大,达96.43%。
图2:中国公立医疗机构终端咪达唑仑的企业竞争格局
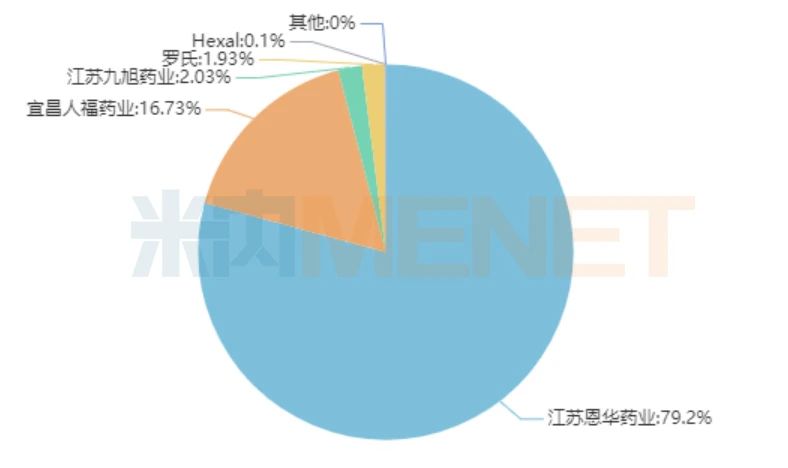
来源:中国公立医疗机构终端竞争格局
恩华药业是该品种的领军企业,2019年的市场份额达79.2%,拥有产品包括了咪达唑仑注射液、马来酸咪达唑仑片。
图3:盐酸咪达唑仑糖浆的市场情况
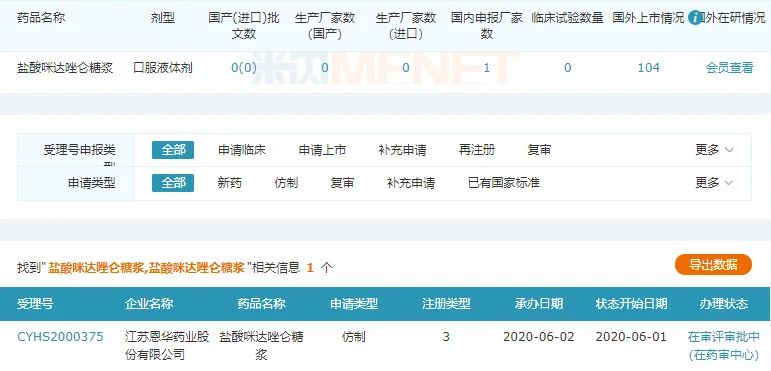
来源:米内网一键检索
拟纳入优先审评的盐酸咪达唑仑糖浆目前市场上暂无企业获批,恩华药业是独家申报,注册分类为3类仿制,若顺利获批则视同过评,该产品上市后,有望提高该公司在咪达唑仑市场的领军优势。
(以上信息来源于医药网)
新闻中心

 琼公网安备 46010602000893号
琼公网安备 46010602000893号
